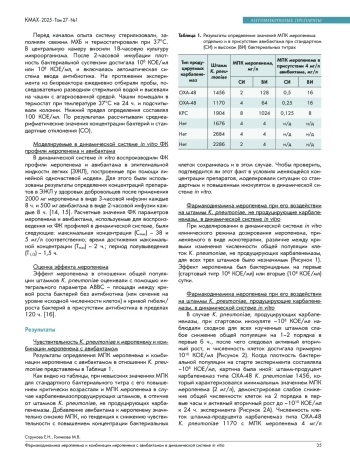
Цель. Изучение фармакодинамики меропенема при его применении отдельно и в комбинации с авибактамом в динамической системе in vitro; оценка эффективности меропенема при его действии на штаммы K. pneumoniae, продуцирующие и не продуцирующие карбапенемазы; изучение влияния концентрации бактерий на активность меропенема и его эффект.
Материалы и методы. Штаммы K. pneumoniae, продуцирующие карбапенемазы типа KPC и OXA- 48, и штаммы, не продуцирующие карбапенемазы, подвергали воздействию меропенема или его комбинации с авибактамом (только продуценты карбапенемаз) в модифицированной динамической системе in vitro диализного типа, воспроизводящей фармакокинетические профили препаратов в легких человека при ежедневном 3-кратном введении на протяжении 5 суток. Оценивали эффект препаратов в отношении общей популяции K. pneumoniae при разных стартовых бактериальных титрах (106 и 108 КОЕ/мл) путем высева проб на твердые среды.
Результаты. В динамической системе in vitro эффект меропенема был бактерицидным для штаммов K. pneumoniae, не продуцирующих карбапенемазы, с МПК 2-4 мг/л, в то время как штаммы-продуценты карбапенемаз с сопоставимыми МПК меропенема преимущественно демонстрировали быстрый вторичный рост как при высокой, так и при низкой стартовой концентрации бактерий в эксперименте. Добавление авибактама приводило к усилению эффекта меропенема и снижению численности клеток всех штаммов-продуцентов при обоих стартовых инокулятах.
Выводы. На основании данных о чувствительности штаммов K. pneumoniae к меропенему, но без проверки их способности к продукции карбапенемаз, невозможно гарантировать успешный исход терапии карбапенемами как при низком (имитация легкой инфекции), так и при высоком (имитация тяжелой инфекции) стартовом титре бактерий. Добавление авибактама позволило значительно усилить эффект меропенема в отношении всех продуцентов карбапенемаз.
Идентификаторы и классификаторы
- SCI
- Биология
Распространение микроорганизмов, устойчивых к бета-лактамным антибиотикам, является глобальной проблемой современной антибиотикотерапии. Как правило, это штаммы, способные к продукции бета-лактамаз – ферментов, разрушающих бета-лактамные антибиотики, в том числе и карбапенемы. Последние в свою очередь являются препаратами первой линии и применяются при лечении пациентов с тяжелыми инфекционными заболеваниями. В клинике значение минимальной подавляющей концентрации (МПК) является единственным ориентиром, на основании которого врач может разработать стратегию антибиотикотерапии.
Список литературы
1. Abodakpi H., Chang K.T., Sánchez Díaz A.M., Cantón R., Lasco T.M., Chan K., et al. Prevalence of extendedspectrum beta-lactamase and carbapenemase-producing bloodstream isolates of Klebsiella pneumoniae in a tertiary care hospital. J Chemother. 2018;30(2):115-119. DOI: 10.1080/1120009X.2017.1399233
2. Fattouh R., Tijet N., McGeer A., Poutanen S.M., Melano R.G., Patel S.N. What is the appropriate meropenem MIC for screening of carbapenemaseproducing Enterobacteriaceae in low-prevalence settings? Antimicrob Agents Chemother. 2015;28;60(3):1556-1559. DOI: 10.1128/AAC.02304-1
3. European Committee on Antimicrobial Susceptibility testing (EUCAST). Breakpoint tables for interpretation of MICs and zone diameters. Ver. 14.0 2024. Available at: www.eucast.org/clinical_breakpoints/. Accessed November 12, 2024.
4. Esterly J.S., Wagner J., McLaughlin M.M., Postelnick M.J., Qi C., Scheetz M.H. Evaluation of clinical outcomes in patients with bloodstream infections due to gram-negative bacteria according to carbapenem MIC stratification. Antimicrob Agents Chemother. 2012;56:4885-4890. DOI: 10.1128/AAC.06365-11
5. Robert J., Pantel A., Merens A., Meiller E., Lavigne J.P., Nicolas-Chanoine M.H.; ONERBA’s carbapenem resistance study group. Development of an algorithm for phenotypic screening of carbapenemase-producing Enterobacteriaceae in the routine laboratory. BMC Infect Dis. 2017;7(1):78. DOI: 10.1186/s12879-016-2174-y
6. Белобородов В.Б., Гусаров В.Г., Дехнич А.В., Замятин М.Н., Зубарева Н.А., Зырянов С.К. и соавт. Методические рекомендации “Диагностика и антимикробная терапия инфекций, вызванных полирезистентными микроорганизмами”. Утверждены 11.10.2019 г. Доступно по адресу: http://antibiotics.ru/files/pdf/2019/guidelines-daticmm-20191204.pdf. Ссылка активна на 12 ноября 2024 г.
7. Alieva K.N., Golikova M.V., Dovzhenko S.A., Kobrin M.B., Strukova E.N., Ageevets V.A., et al. Testing the mutant selection window hypothesis with meropenem: in vitro model study with OXA-48-producing Klebsiella pneumoniae. PLoS One. 2023;18(8):e0288660. DOI: 10.1371/journal.pone.0288660
8. Burgess D.S., Hall 2nd R.G. In vitro killing of parenteral beta-lactams against standard and high inocula of extended-spectrum beta-lactamases and non-ESBL producing Klebsiella pneumoniae. Diagn Microbiol Infect Dis. 2004;49:41-46. DOI: 10.1016/j.diagmicrobio.2003.11.007
9. Национальный стандарт Российской Федерации ГОСТ Р ИСО 20776-1-2022. Исследование чувствительности инфекционных агентов, и оценка функциональных характеристик изделий для исследования чувствительности к антимикробным средствам. Часть 1. Референтный метод микроразведений в бульоне для лабораторного исследования активности антимикробных агентов по отношению к быстрорастущим аэробным бактериям, вызывающим инфекционные заболевания. Доступно по адресу: https://rosgosts. ru/file/gost/11/100/gost_r_iso_20776-1-2022.pdf. Ссылка активна на 12 ноября 2024 г.
10. Wilson G.M., Fitzpatrick M., Walding K., Gonzalez B., Schweizer M.L., Suda K.J., et al. Meta-analysis of clinical outcomes using ceftazidime/avibactam, ceftolozane/tazobactam, and meropenem/vaborbactam for the treatment of multidrug-resistant Gram-negative infections. Open Forum Infect Dis. 2021;8(2):651. DOI: 10.1093/ofid/ofaa651
11. Vázquez-Ucha J.C., Arca-Suárez J., Bou G., Beceiro A. New carbapenemase inhibitors: clearing the way for the beta-lactams. Int J Mol Sci. 2020;21(23):9308. DOI: 10.3390/ijms21239308
12. Yahav D., Giske C.G., Grāmatniece A., Abodakpi H., Tam V.H., Leibovici L. New β-lactam-β-lactamase inhibitor combinations. Clin Microbiol Rev. 2020;34:e00115-20. DOI: 10.1128/CMR.00115-20
13. Патент № RU 2787393. Голикова М. В., Фирсов А.А., Струкова Е.Н., Портной Ю.А. Модифицированная динамическая система in vitro (м-дс) для фармакокинетико-фармакодинамических исследований с антимикробными препаратами. Доступно по адресу: https://yandex.ru/patents/doc/RU2787393C1_20230109. Ссылка активна на 12 ноября 2024 г.
14. Nicolau D.P., Siew L., Armstrong J., Li J., Edeki T., Learoyd M., Das S. Phase 1 study assessing the steady-state concentration of ceftazidime and avibactam in plasma and epithelial lining fluid following two dosing regimens. J Antimicrob Chemother. 2015;70(10):2862-2869. DOI: 10.1093/jac/dkv170
15. Wenzler E., Gotfried M.H., Loutit J.S., Durso S., Griffith D.C., Dudley M.N., Rodvold K.A. MeropenemRPX7009 concentrations in plasma, epithelial lining fluid, and alveolar macrophages of healthy adult subjects. Antimicrob Agents Chemother. 2015;59(12):7232-7239. DOI: 10.1128/AAC.01713-15
16. Firsov A.A., Zinner S.H., Vostrov S.N., Portnoy Y.A., Lubenko I.Y. AUC/MIC relationships to different endpoints of the antimicrobial effect: multiple-dose in vitro simulations with moxifloxacin and levofloxacin. J Antimicrob Chemother. 2002;50:533-539. DOI: 10.1128/AAC.47.5.1604-1613.2003
17. Zhao Q., Sha L., Wu Z., Meng L., Yang F., Wu L., et al. Evolution of carbapenem resistance in Klebsiella pneumoniae and Escherichia coli carrying bla(NDM-1) gene: imipenem exposure results in sustained resistance memory of strains in vitro. Ann Clin Microbiol Antimicrob. 2023;12;22(1):46. DOI: 10.1186/s12941-023-00598-8
18. Lenhard J.R., Bulman Z.P. Inoculum effect of β-lactam antibiotics. J Antimicrob Chemother. 2019;74(10):2825-2843. DOI: 10.1093/jac/dkz226
19. Weisenberg S.A., Morgan D.J., Espinal-Witter R., Larone D.H. Clinical outcomes of patients with Klebsiella pneumoniae carbapenemase producing K. pneumoniae after treatment with imipenem or meropenem. Diagn Microbiol Infect Dis. 2009;64:233-235. DOI: 10.1016/j.diagmicrobio.2009.02.004
20. Oliva A., Al Ismail D., Arcari G., Miele M.C., Casali E., Sacco F., et al. Ceftazidime/avibactam-resistant meropenem-susceptible KPC-producing Klebsiella pneumoniae: analysis of cases and evaluation of in vitro activity of fosfomycin-containing combinations. J Glob Antimicrob Resist. 2023;33:321-327. DOI: 10.1016/j.jgar.2023.03.012
21. Cordovana M., Kostrzewa M., Sóki J., Witt E., Ambretti S., Pranada A.B. Bacteroides fragilis: a whole MALDI-based workflow from identification to confirmation of carbapenemase production for routine laboratories. Anaerobe. 2018;54:246-253. DOI: 10.1016/j.anaerobe.2018.04.004
22. Allander L., Vickberg K., Fermér E., Söderhäll T., Sandegren L., Lagerbäck P., Tängdén T. Impact of porin deficiency on the synergistic potential of colistin in combination with β-lactam/β-lactamase inhibitors against ESBLand carbapenemase-producing Klebsiella pneumoniae. Antimicrob Agents Chemother. 2024;6;68(11): e0076224. DOI: 10.1128/aac.00762-24
23. El Hafi B., Rasheed S.S., Abou Fayad A.G., Araj G.F., Matar G.M. Evaluating the efficacies of carbapenem/β-lactamase inhibitors against carbapenem-resistant gramnegative bacteria in vitro and in vivo. Front Microbiol. 2019;10:933. DOI: 10.3389/fmicb.2019.00933
24. Li X., Chen Z., Jiao J., Wang S., Wang Y., Wu W., et al. In vitro and in vivo activity of meropenem+avibactam against MBL-producing carbapenem-resistant Klebsiella pneumoniae. Expert Rev Anti Infect Ther. 2023;21(1):91-98. DOI: 10.1080/14787210.2022.2153117
25. Tumbarello M., Trecarichi E.M., Corona A., De Rosa F.G., Bassetti M., Mussini C., et al. Efficacy of ceftazidime-avibactam salvage therapy in patients with infections caused by Klebsiella pneumoniae carbapenemase-producing K. pneumoniae. Clin Infect Dis. 2019;68(3):355-364. DOI: 10.1093/cid/ciy492
Выпуск
Другие статьи выпуска
Цель. Изучить особенности микробного пейзажа у пациентов с хронической обструктивной болезнью легких и хроническим простым бронхитом профессиональной этиологии (ХОБЛ ПЭ и ХПБ ПЭ) от воздействия минеральной пыли с различными клиническими фенотипами.
Материалы и методы. В зависимости от частоты обострений и показателя спирометрии пациенты были разделены на 3 группы: клинический фенотип «В» (ХОБЛ ПЭ, GOLD II) – 10 человек; клинический фенотип «Е» (ХОБЛ ПЭ, GOLD III-IV) – 19 человек; ХПБ ПЭ – 11 человек. В соответствии с методическими указаниями осуществлялся забор слизи из лакун миндалин, далее биоматериал транспортировался в лабораторию в изотермических условиях с использованием транспортной среды Эймса. Посев осуществлялся на плотные питательные среды, которые инкубировались в аэробных и микроаэрофильных условиях. Идентификацию выросших культур проводили с использованием метода MALDI-ToF масс-спектрометрии. Антибиотикорезистеность выделенных микроорганизмов определяли диско-диффузионным методом в соответствии с актуальной версией рекомендаций МАКМАХ.
Результаты. Общими характеристиками микробиоты у пациентов ХОБЛ ПЭ обоих фенотипов были: преобладание представителей Firmicutes, равная бактериальная нагрузка (р = 0,48), отсутствие протективных комменсалов и типичных для больных ХОБЛ микроорганизмов (Moraxella catarrhalis). Streptococcus pneumoniae и Haemophilus influenzae встретились только у одного пациента фенотипа «Е». Фенотип ХОБЛ ПЭ «Е» качественно отличался от фенотипа «В» за счет преобладания представителей Pseudomonadota (р = 0,0005), условно-патогенных микроорганизмов над непатогенными (54% против 19%, р = 0,0005), меньшим количеством представителей Neisseriales, большим количеством устойчивых к антибиотикам микроорганизмов и большим количеством грибов рода Candida.
Выводы. Результаты исследования указывают на гетерогенность микробиоты у различных клинических фенотипов пациентов ХОБЛ ПЭ и ХПБ ПЭ. Общими чертами всех фенотипов стала тенденция к росту условно-патогенной микробиоты, наличие устойчивых к антибиотикам изолятов. Пациенты с частыми обострениями имели эндотип Т2 воспаления, у них отмечалось более выраженное упрощение микробиоты, рост представителей условно-патогенной микробиоты, устойчивой к антибиотикам. Нарушения в микробиоте у пациентов с ХПБ ПЭ говорят о вовлечении микроорганизмов в процессы воспаления и ремоделирования дыхательных путей на раннем этапе заболевания, что требует дальнейших исследований. Полученные результаты необходимо учитывать при проведении эмпирической антибактериальной терапии обострений у этих больных, а также включении в реабилитационную программу пациентов ХОБЛ ПЭ и ХПБ ПЭ вакцинопрофилактики против пневмококка.
Цель. Провести анализ чувствительности стрептококков различных видов к антибактериальным препаратам в отделениях многопрофильного стационара. Материалы и методы. Проведено эпидемиологическое наблюдательное описательное сплошное ретроспективное исследование. Проанализированы данные чувствительности к антибиотикам 2916 изолятов стрептококков, вне зависимости от их клинической значимости, полученных из лабораторной информационной системы «АЛИСА» ГКБ №67 им. Л. А. Ворохобова ДЗМ за период с 01.01.2017 по 31.12.2022. Исследование чувствительности стрептококков к антибиотикам проводили методом микроразведений на микробиологическом анализаторе BD Phoenix M50 в соответствии с рекомендациями EUCAST (v.2.1-v12.0, в зависимости от года тестирования изолята). Статистическую обработку с использованием программ Microsoft Excel 2010 и IBM SPSS Statistics22.
Результаты. Видовой состав выделенных стрептококков различался в зависимости от отделения. В отделении гнойной хирургии за анализируемый период чаще выделялись: S. pyogenes (28,5%), S. agalactiae (22,0%), S. anginosus (16,5%); в отделении колопроктологии – S. anginosus (41,7%), S. constellatus (16,0%), S. agalactiae (14,5%); в хирургическом отделении – S. anginosus (40,1%) и S. constellatus (31,4%); в реанимационном отделении – S. anginosus (21,8%), S. constellatus (11,3%), S. oralis (11,1%); в гинекологическом отделении – S. agalactiae (49,9%) и S. anginosus (31,3%). Значительная доля культур S. agalactiae проявляла резистентность к тетрациклину и клиндамицину во всех отделениях больницы. В отделении гнойной хирургии с 2019 г. по 2021 г. был отмечен рост устойчивости S. agalactiae к эритромицину с 15,4% до 38,3%, а в отделении колопроктологии – с 16,7% до 38,5%; также возросла устойчивость и к клиндамицину с 2018 г. по 2020 г, в гнойной хирургии с 24,2% до 71,3%, в колопроктологии – с 13,6 до 70,7%, в гинекологии – с 20,0 до 90,3%. В реанимационном отделении S. agalactiae и S. pyogenes были наиболее устойчивы к тетрациклину (79,5% и 51,3%), эритромицину (32,8% и 31,7%) и триметоприму-сульфаметоксазолу (18,5% и 26,8%). S. pneumoniae проявлял наибольший уровень резистентности к действию эритромицина (35,3%), клиндамицина (29,3%) и триметоприма-сульфаметоксазола (26,0%).
Выводы. Выявлен рост устойчивости к антимикробным препаратам у наиболее часто встречающихся видов стрептококков. Обнаружена неодинаковая чувствительность к антибиотикам стрептококков одного и того же вида в различных отделениях стационара. Отмечена тенденция к увеличению распространенности полирезистентных штаммов S. pyogenes и S. agalactiae в реанимационном и гнойно-хирургическом отделениях.
Цель. Изучить микробный состав биоптатов при воспалительных заболеваниях кишечника.
Материалы и методы. С ноября 2019 по февраль 2023 г. обследовано 100 пациентов колопроктологического отделения с воспалительными заболеваниями кишечника (ВЗК): 65 пациентов – с язвенным колитом и 35 пациентов с болезнью Крона. Осуществлен метагеномный анализ биоптатов (ДНК-секвенатор Illumina, США), полученных в ходе эндоскопического исследования по стандартной методике, с биоиформатическим анализом данных. Разнообразие микробиомов в образцах (альфа-разнообразие) оценивали с помощью индекса Фишера. С помощью расстояния Брея-Кертиса оценивали сходство микробиомов между образцами (бета-разнообразие). Проведен анализ главных координат (PCoA) для визуализации сходства микробиомов между образцами. Статистически значимыми считали результаты при p < 0,05.
Результаты. Метагеномный анализ позволил изучить качественный и количественный состав микробиоты кишечника у пациентов с язвенным колитом и болезнью Крона. Выявлено 20 филумов микроорганизмов, в том числе 146 семейств, 336 родов, 516 видов микроорганизмов. На уровне филумов было получено два основных – Proteobacteria, Firmicutes. При сравнии изучаемые нозологические формы между собой было отмечено увеличение разнообразия бактерий филума Proteobacteria в 1,2 раза при язвенном колите. Преобладающим видом данного филума является Escherichia сoli. В свою очередь, относительная представленность кишечной палочки выше в 1,6 раз у пациентов с болезнью Крона (23,9%/14,48%). Выявлены таксономические категории, отсутствующие при том или ином виде заболевания – отделы: Cyanobacteria (0,049%), Acidobacteria (0,010), Planctomycetes (0,009%), некультивируемые бактерии-кандидаты в подразделении SR1 (Sulfur-River 1) (0,007%), Synergistetes (0,007%), Chloroflexi (0,004%), Lentisphaerae (0,002%), бактерии-кандидаты типа OD1 (Parcubacteria) (0,001%), Spirochaetes (0,001%), род Helicobacter (5%) выявлены только у пациентов с язвенным колитом; отдел Gemmatimonadetes (0,009%) – только при болезни Крона.
Выводы. Идентификация кишечных микроорганизмов, ассоциированных с патогенезом воспалительных заболеваний кишечника, является крайне важным аспектом для глубокого понимания различных патогенных факторов, имеющих большое значение для раннего выявления ВЗК.
Цель. Описать фенотипические и геномные характеристики феномена изменения уровня чувствительности к азтреонаму у клинического изолята Pseudomonas aeruginosa при формировании резистентности к колистину в условиях эволюционного эксперимента.
Материалы и методы. Объектом исследования был клинический изолят P. aeruginosa с фенотипом множественной антибиотикорезистентности. Исследование проводили на основе пространственно-временной модели формирования резистентности подвижных бактерий в возрастающей концентрации колистина. Эксперимент продолжался в течение 44 суток. По мере появления роста бактерий в зонах с повышающейся концентрацией колистина, с фронта распространения P. aeruginosa отбирали образцы в точках опережающего роста. У отобранных изолятов определяли уровни чувствительности к антибиотикам и выявляли геномные изменения.
Результаты. У исходного изолята МПК азтреонама составляла 4 мг/л, что соответствовало критерию EUCAST «чувствительный при увеличенной экспозиции» Из 74 изолятов P. aeruginosa, отобранных в ходе эксперименты, было отобрано 11 изолятов с изменившейся чувствительностью к азтреонаму. У 6 из 11 отобранных изолятов чувствительность к азтреонаму повысилась, у 5 изолятов усилилась резистентность. Генетические детерминанты резистентности, присутствующие в исходном штамме, не изменились. Изоляты, у которых восстановилась чувствительность к азтреонаму, имели набор мутаций, включающих повреждение генов pmrB (del-18bp-298-315) и davD (TGA1450- 1452→CTC). Изоляты, у которых МПК азтреонама увеличилась в 4 раза, несли различные мутационные профили. Изолят с максимальной устойчивостью к азтреонаму (МПК = 32 мг/л) имел мутацию в гене capD (del-T-360) и большую делецию 262 402 bp (239 ORF). Мутации, появлявшиеся в генах phoQ, lpxL_2, wecA, mexB, spaQ, pcpR и rpoA, не оказывали значительного влияния на уровень чувствительности к азтреонаму.
Выводы. Полученные результаты внесли вклад в понимание направлений генно-инженерного моделирования, направленного на расширение представлений о механизмах устойчивости к азтреонаму.
Цель. Определение молекулярно-биологических характеристик штаммов Candida albicans, выделенных при рецидивирующем вульвовагинальном кандидозе (РВВК), ассоциированных с формированием резистентности к препаратам азолового ряда.
Материалы и методы. В исследование было включено 36 клинических изолятов C. albicans от больных РВВК, обратившихся в НИИ медицинской микологии им. П. Н. Кашкина за амбулаторной помощью с июля по ноябрь 2024 г. Видовую идентификацию Candida spp. проводили методами MALDI-TOF масс-спектрометрии и таргетного секвенирования. Чувствительность Candida spp. к противогрибковым лекарственным средствам (ПГЛС) определяли с помощью тест системы Fungus AST (Autobio Diagnostics Co, Китай) с интерпретацией пороговых значений МПК в соответствии с CLSI M27A, 2022. Нуклеотидную последовательность гена ERG11 изучали методом таргетного секвенирования на генетическом анализаторе ABI PRISM 3500. Уровень экспрессии генов белков-транспортеров лекарственных препаратов CDR1, CDR2, MDR1 и FLU1 анализировали в ходе ПЦР-РВ с использованием флуоресцентного красителя EVA Green методом относительных измерений 2-ΔΔСt. Биопленкообразование штаммов C. albicans оценивали по общей клеточной массе (окрашивание водным раствором кристаллического фиолетового) и метаболической активности клеток (метод восстановления солей тетразолия). Статистическую обработку результатов проводили с использованием непараметрических критериев оценки программы SPSS v.22.0.
Результаты. 11 (30,5%) штаммов были чувствительны к флуконазолу, 6 (14,0%) – отнесены к категории «чувствительный дозо-зависимый», 20 (55,5%) – резистентны к данному ПГЛС. Все штаммы были чувствительны к полиенам, эхинокандинам и 5-флуцитозину. В работе показана корреляция между нуклеотидным полиморфизмом гена ERG11 и чувствительностью штамма к флуконазолу. Резистентные штаммы C. albicans (МПК >8 мг/л) отличались наименьшей вариабельностью и наличием в генотипе единственной миссенс-мутации T394C (Y132H), ассоциированной с устойчивостью к азолам. Предположена возможная роль A1343G (E448G), как супрессорной внутригенной мутации, нивелирующей влияние T394C (Y132H) на конформационные изменения белка Erg11. В данном аспекте необходимы дальнейшие исследования. Для генов ERG11 и FLU1 показан повышенный уровень экспрессии (р = 0,004 и р = 0,012 соответственно) у нечувствительных к флуконазолу штаммов C. albicans по сравнению с чувствительными. Статистически значимых различий в экспрессии генов белков-транспортеров лекарственных препаратов CDR1, CDR2 и MDR1 не установлено. Все изученные штаммы C. albicans образовывали биопленки in vitro. Штаммы, резистентные к флуконазолу, обладали большей метаболической активностью и клеточной массой биопленки (p = 0,011 и р = 0,012 соответственно).
Выводы. Резистентность возбудителей РВВК в Северо-Западном регионе России ассоциирована с повышенным биопленкообразованием, аминокислотной заменой Y132H и повышенным уровнем экспрессии генов ERG11 и FLU1.
Цель. Разработать модель количественной оценки экономических потерь, обусловленных нерациональным применением антимикробных препаратов и недостаточной точностью микробиологической диагностики антимикробной резистентности.
Материалы и методы. Для формирования стартовых параметров модели было проведено анкетирование по особенностям практики антимикробной терапии, значении микробиологических заключений с оценкой частоты ошибок и их последствий. Основа модели представляет взаимосвязь между точностью микробиологического заключения, вероятностью нерациональной антимикробной терапии и экономическим ущербом. С целью повышения точности и адаптивности модели были включены параметры валового регионального продукта, численность населения, структура ключевых возбудителей внебольничных и нозокомиальных инфекций, частота различных фенотипов, а также цены на антимикробные препараты.
Результаты. Бактериальные инфекции встречаются на регулярной основе в практике более 75% специалистов. В наибольшем проценте случаев на запрос консультации клинического фармаколога по вопросам терапии инфекций влияет множественная лекарственная устойчивость патогенов и неэффективность назначенной терапии. Электронное микробиологическое заключение получают 50,85% специалистов, а 65,62% – результаты из внутренней лаборатории. Однако 36% специалистов не имеют доступа к консультации специалистов лабораторной службы. Наличие связи между интерпретацией антибиотикограммы и выбором антимикробной терапии отметили 82,32% специалистов. На амбулаторном этапе легкие и умеренные последствия некорректной антимикробной терапии (АМТ) с частотой до 25% наблюдают 25,6% и 79,85% специалистов соответственно. На стационарном этапе умеренные и тяжелые последствия АМТ (частота более 25%) регистрируют 34,83% и 19,52% специалистов. Согласно разработанной модели на 1000 пациентов, вероятности ошибки 10% и с учетом заданных параметров, прямые расходы на стационарном треке составляют более 1,7 млн рублей, а общие потери достигают 18,94 млн рублей.
Выводы. Созданная экономическая модель позволяет оценить экономические последствия нерациональной антимикробной терапии, учитывая как прямые, так и косвенные затраты, и демонстрирует высокую адаптивность с учетом различных факторов. Полученные результаты подчеркивают необходимость дальнейших исследований для улучшения взаимодействия специалистов и разработки стратегий по снижению экономических потерь от антибиотикорезистентности.
Целью резолюции являлась выработка согласованной экспертной позиции по проблемным вопросам организации стратегии контроля антибиотикорезистентности и рационального применения антибактериальных препаратов.
29 мая 2025 г. состоялось заседание Совета экспертов «Цефиксим (современный пероральный цефалоспорин III поколения компании Сандоз) и его место в клинической практике», в состав которого вошли представители ведущих российских научно-исследовательских и образовательных медицинских учреждений, ведущие эксперты в области антибиотикорезистентности, пульмонологии, оторинолариногологии и педиатрии: академик РАН, доктор медицинских наук, профессор С. Н. Авдеев, член-корр. РАН, доктор медицинских наук, профессор Р. С. Козлов, доктор медицинских наук, профессор В. М. Свистушкин, доктор медицинских наук, профессор А. И. Синопальников, доктор медицинских наук, профессор О. В. Зайцева, доктор медицинских наук, профессор И. Н. Захарова, доктор медицинских наук, профессор С. К. Зырянов, доктор медицинских наук, профессор Е. П. Карпова, доктор медицинских наук, профессор Г. Н. Никифорова, доктор медицинских наук, профессор С. В. Рязанцев, кандидат медицинских наук И. В. Андреева, кандидат медицинских наук А. В. Дехнич, кандидат медицинских наук Е. В. Довгань, кандидат медицинских наук О. У. Стецюк.
В этом обзоре литературы обобщены актуальные данные по использованию антиинфекционных средств при лечении абсцессов головного мозга, в частности, оториносинусогенных. Проанализированы в основном наиболее крупные публикации преимущественно последнего десятилетия, посвященные рассматриваемой проблеме. Поиск проводился по ключевым словам в базе данных PubMed. Мультидисциплинарный, командный подход с участием клинического фармаколога повышает вероятность успешного лечения интракраниальных абсцессов. При этом выбор антибиотиков должен учитывать локальные данные по антибиотикорезистентности, что в текущей литературе пока не нашло широкого отражения.
В статье проведен анализ статистических данных заболеваемости дифтерией на территории России конца ХХ – начала ХХI в., приведены абсолютные и относительные интенсивные показатели заболеваемости в целом в стране, рассмотрены закономерности развития эпидемического процесса, определена роль популяционного антитоксического поствакцинального иммунитета в борьбе с этой грозной инфекцией. Дана сравнительная характеристика заболеваемости в различных возрастных группах населения, а также иммунологического статуса всех возрастных групп, был сделан вывод о снижении иммунитета против дифтерии именно за счет взрослого контингента. Так, к 1975 г. в СССР было зарегистрировано 198 случаев дифтерии. Однако, начиная с 1976 г. заболеваемость начала стремительно расти и достигла пика к 1985 г., когда среди взрослого населения уровень иммунитета не превышал 25%. В 1990-х гг. отмечен новый подъем с пиком, зарегистрированным в 1994 г., когда всего заболело около 40 тыс. человек. С 1990 по 1996 г. дифтерией заболело 111154 человека, из них 35928 детей, 15776 подростков и 59450 взрослых; умерло 3047 человек, из них 729 детей, 37 подростков и 2281 взрослых. Далее прививками было охвачено свыше 80 млн человек, что составило около 90% взрослого населения. В результате было достигнуто значительное снижение заболеваемости, которая, начиная с 2003 г., достигла показателей спорадической, и к 2023 г. интенсивный показатель установился на уровне тысячных долей на 100 тыс. населения. Однако, не смотря на снижение общей заболеваемости дифтерией в стране, она остается актуальной социально-значимой проблемой практического здравоохранения.
В данном обзоре представлена характеристика представителей рода Weissella, в частности, W. confusa, W. cibaria и W. viridescens. Рассмотрены морфологические, культуральные, биохимические свойства данных микроорганизмов, входящих в род Weissella. Описаны особенности микроэкологии, сложности идентификации данных микроорганизмов в клинической практике. Рассмотрены клинические случаи, вызванные инфицированием представителями рода Weissella, особенности проявления и течения заболеваний, обусловленные данными возбудителями. Установлено, что микроорганизмы, относящиеся к роду Weissella, представляют опасность для иммунокомпрометированных пациентов, страдающих хроническими заболеваниями, перенесших трансплантацию гемопоэтических стволовых клеток, печени и кожных лоскутов, а также пожилых пациентов. Установлено, что представители рода Weissella обладают устойчивостью к антибиотикам, таким как ванкомицин, цефотаксим, левофлоксацин, метронидазол, тейкопланин, имипенем и меропенем.
Цель. Определить роль ферритина (ФТ), прокальцитонина (ПКТ) и их соотношения (ФТ/ПКТ) в дифференциальной диагностике вирусного поражения легких и бактериальной внебольничной пневмонии (ВП).
Материалы и методы. В проспективное многоцентровое исследование включали взрослых пациентов с ВП, госпитализированных в многопрофильные стационары с июля по ноябрь 2023 г. Этиологическая диагностика включала микробиологическое исследование респираторного образца и крови (при тяжелом течении), экспресс-тесты на пневмококковую и легионеллезную антигенурию, а также молекулярное исследование респираторных образцов для выявления ДНК/РНК наиболее распространенных респираторных вирусов и трудно- или некультивируемых бактериальных возбудителей. У всех пациентов в дополнение к стандартному протоколу обследования определяли уровень ПКТ и ФТ.
Результаты. Из 152 обследованных пациентов клинически значимые возбудители обнаружены в 96 случаях, в т. ч. вирусы в 28 (29%), бактериальные возбудители в 52 (54%), ассоциации бактерий и вирусов в 16 (17%). Среди бактериальных возбудителей значительную долю (62%) занимала Mycoplasmoides pneumoniae. Сравнительный анализ пациентов с ВП бактериальной этиологии и вирусным поражением легких выявил более низкий уровень ФТ при инфицировании вирусами (127,5 против 242 мкг/л, p = 0,013), значимых различий при оценке ПКТ и соотношения ФТ/ПКТ не получено. После исключения случаев инфицирования M. pneumoniae сохранялись значимые различия ФТ – 127,5 против 338,5 мкг/л (p = 0,002), а также ПКТ – 0,1 против 0,4 нг/мл (p = 0,01). Пороговые значения ФТ >146 мкг/л (AUC = 0,76; ОШ = 8,0) и ПКТ > 0,15 нг/мл (AUC = 0,70; ОШ = 5,4) обладали прогностической ценностью для диагностики бактериальной ВП при исключении случаев инфицирования M. pneumoniae. Удвоение уровня ФТ и ПКТ ассоциировалось с повышением вероятности бактериальной ВП в 1,8 (95% ДИ: 1,3–2,9) и 1,23 (95% ДИ: 1,05–1,48) раза соответственно.
Выводы. Исследование соотношения ФТ/ПКТ не обладало достаточной диагностической точностью в дифференциации вирусного поражения легких и бактериальной ВП у взрослых пациентов в нашей популяции; при оценке ПКТ были получены значимые статистически, но не клинически значения, а определение ФТ продемонстрировало определенную диагностическую ценность, однако, для надежного использования данного биомаркера в клинической практике необходимы более крупные исследования с сопоставимыми по тяжести группами пациентов.
Антибактериальная терапия у пациентов с инфекциями мочевых путей составляет неотъемлемую часть лечения, зачастую являясь единственным этиопатогенетическим его компонентом. При этом рациональность выбора антимикробного препарата зависит как от чувствительности основных возбудителей заболевания, так и от фармакокинетических и фармакодинамических особенностей данного класса лекарственных средств. В статье приведены сведения о четвертьвековом мониторинге этиологической структуры и чувствительности уропатогенов в России, обоснованы рекомендации по выбору препаратов нитрофуранового ряда при неосложненном остром цистите.
Издательство
- Издательство
- МАКМАХ
- Регион
- Россия, Смоленск
- Почтовый адрес
- 214019, Россия, Смоленск, а/я 5
- Юр. адрес
- 214019, Смоленская обл, г Смоленск, ул Крупской, д 28
- ФИО
- Козлов Роман Сергеевич (ПРЕЗИДЕНТ)
- Контактный телефон
- +7 (___) _______